
Los lubricantes se envejecen y alteran químicamente por un proceso llamado oxidación. De hecho, la oxidación es el principal mecanismo por el cual el lubricante se degrada en el tiempo bajo condiciones normales de operación. Típicamente es el resultado del deterioro de las propiedades físicas y químicas del aceite básico y de los aditivos. Entender cómo un lubricante se oxida es esencial para prevenir, retardar y monitorear el proceso.
A medida que el aceite es utilizado en una máquina, se produce el proceso de oxidación, que típicamente comienza con el agotamiento de los aditivos antioxidantes. Si las condiciones que producen este estrés sobre el lubricante permanecen sin cambios, los aditivos se agotarán casi en una forma lineal. Esto comúnmente se conoce como el periodo de inducción. Cuando en gran parte los inhibidores de oxidación se han agotado, se alcanza el punto de quiebre del lubricante, momento en el cual el lubricante ha perdido su primera línea de defensa contra la oxidación.
Algunas bases lubricantes son muy robustas y resisten la oxidación de forma natural. Aquí se incluyen la mayoría de los sintéticos. Sin embargo, si la exposición a compuestos pro-oxidantes como una alta temperatura, la humedad, las partículas metálicas, la agitación y el oxígeno es bastante severa, aún los sintéticos más robustos darán lugar a la oxidación.
El proceso de oxidación tiene el potencial de presentarse casi espontáneamente, aun en un aceite almacenado en su contenedor. Sin embargo, la velocidad con que los aditivos se agotan y se oxida la base lubricante generalmente se correlaciona con la intensidad de los pro-oxidantes que existen en el aceite. Finalmente, las consecuencias de este proceso químico incluirán un incremento en la viscosidad del aceite y en los ácidos orgánicos; la formación de lodos, barniz y depósitos; agotamiento de aditivos (incluyendo antidesgaste, dispersantes, inhibidores de corrosión, etc.); y la pérdida de otras propiedades vitales para el desempeño del aceite. Una vez que se presentan estas condiciones indeseables en el aceite, la máquina no estará protegida efectivamente contra la fricción, el desgaste y la corrosión.
Una revisión de la oxidación
La oxidación es una serie de complejas reacciones en cadena. Para entender mejor el proceso, siga el ejemplo de la gráfica 1, donde se explica cada elemento.
El proceso de oxidación consiste de tres etapas clave: iniciación, propagación y terminación.
La etapa de iniciación describe el mecanismo mediante el cual los componentes del lubricante se combinan químicamente con uno más catalizadores para producir radicales libres (los radicales libres son moléculas altamente reactivas que intentan encontrar otras moléculas para combinarse y crear nuevos productos).
La propagación se refiere a la complejidad de reacciones adicionales de varios tipos de radicales libres y catalizadores que dan como resultado la producción de más radicales libres y compuestos oxigenados.
La terminación involucra la eventual finalización del proceso de oxidación, ya sea esta negativa o positivamente. Si es negativa, los antioxidantes se han agotado y el proceso de oxidación continuará. Si es positiva, los antioxidantes posiblemente han detenido el progreso de la oxidación. Tenga presente que los antioxidantes son sacrificables, lo que significa que ellos comienzan a degradarse a medida que hacen su trabajo. De ahí que el efecto positivo de los antioxidantes se acabará, mientras que el proceso de oxidación total no.
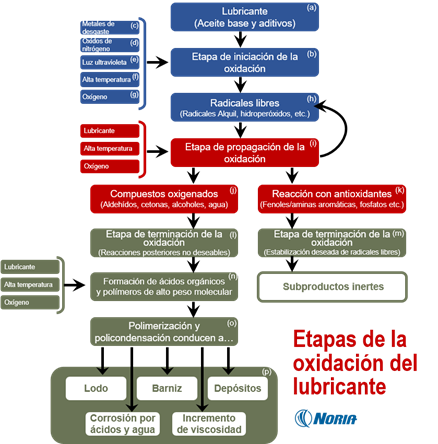
Etapas de la oxidación
El lubricante (a), que es una formulación de bases lubricantes y aditivos, está sujeto en algún momento a condiciones y catalizadores que permiten que inicie de la oxidación. Tanto la base lubricante como los aditivos actúan contra el proceso de oxidación y están eventualmente sujetos a degradarse.
Durante la etapa de iniciación (b), las moléculas de la base lubricante reaccionan con varios catalizadores, conduciendo a la formación de radicales libres. Una vez que esto ha ocurrido, se inicia una secuencia de oxidación que continua mientras existe el progreso de los radicales libres hacia la etapa de propagación.
Los metales de desgaste (c), tienen el potencial para causar o acelerar las reacciones de oxidación por medio de iones metálicos de cobre, cobalto, cromo, hierro y otros metales de transición. De esta forma, la oxidación no solo tiene la habilidad de crear partículas de desgaste, sino que estas partículas pueden dar origen a otro ciclo para promover procesos de oxidación adicionales.
Los óxidos de nitrógeno (d), como el dióxido de nitrógeno, el óxido nítrico y óxidos nitrosos son otra forma de prooxidantes que catalizan las reacciones de oxidación.
La radiación ultravioleta (e), en forma de luz solar, puede dar inicio a reacciones de oxidación. Esto se observa frecuentemente y a menudo explica la decoloración de un aceite nuevo.
Las elevadas temperaturas (f), promueven y algunas veces son necesarias para que se den ciertas etapas del proceso de oxidación. Cuando se combinan con partículas metálicas u oxígeno, su efecto se multiplica. Si la temperatura es baja, la reacción en cadena generalmente es lenta, pero se incrementa moderadamente por encima de los 100°C.
El oxígeno (g), es el principal catalizador de la oxidación. Está presente en el aire y en otras moléculas como el agua y es parte integral del proceso de oxidación en casi todas las etapas.
Los radicales libres (h) están entre los resultados menos deseados de las reacciones intermedias de la oxidación. Estos fragmentos moleculares altamente reactivos contienen uno o más electrones libres que están propensos a reaccionar con el hidrocarburo u otras moléculas. Algunos radicales libres existen como grupos alquil, hidroperóxido, alquiloxi, hidroxi, alquilperoxi, etc.
Una vez que estos radicales libres están presentes comienzan nuevamente a reaccionar rápidamente –proceso de propagación (i)– con los hidrocarburos y a disolver o liberar oxígeno para formar más radicales libres o compuestos oxigenados. Las altas temperaturas también juegan un papel importante para que se lleven a cabo estas reacciones a niveles más elevados. Otro ejemplo de propagación de la oxidación sería el de la reacción de los radicales peroxi con hidrocarburos para producir hidroperóxidos y más radicales alquil.
Como producto de algunas de esas reacciones en cadena durante la etapa de propagación, se forman compuestos oxigenados como aldehídos, cetonas, alcoholes y agua. Estos productos son el resultado de la reacción entre los radicales alquiloxi y el hidrocarburo.
Los alquil hidroperóxidos y los radicales alquilperoxi pueden ser neutralizados y removidos de la propagación de la oxidación cuando entran en contacto con los antioxidantes (k). La mayoría de los antioxidantes más comunes actúan rompiendo o descomponiendo las reacciones en cadena.
La oxidación se puede iniciar desfavorablemente (l) antes de la etapa de propagación cuando los compuestos oxigenados continúan reaccionando con los hidrocarburos y el oxígeno. De otra forma la oxidación puede terminar favorablemente (m) cuando se estabilizan los radicales libres. Los antioxidantes que rompen cadenas, como los fenoles y las aminas aromáticas, reaccionan con los radicales libres para formar radicales estables y productos inertes. Los antioxidantes del tipo que descomponen los peróxidos, como los fosfatos y sulfitos, reaccionan con ellos para producir alcoholes y agua.
Los compuestos oxigenados (n) reaccionarán adicionalmente con el oxígeno dando como resultados ácidos carboxílicos, ésteres y agua. Este proceso se acelera cuando está sometido a altas temperaturas. Los ácidos carboxílicos se forman en gran parte por la oxidación de los aldehídos y cetonas, que continúan mediante la abstracción de un hidrógeno alfa o hidrógeno aldehídico de las moléculas del hidrocarburo.
La policondensación y polimerización (o) de los compuestos oxigenados describe los efectos de la etapa final de la oxidación.
El incremento en el peso molecular de los compuestos se traduce en formación de lodos, barniz y depósitos. No solo se forman estos productos insolubles, sino que los ácidos orgánicos corroen las superficies juntamente con el agua. La mayoría de los aditivos también se ven afectados negativamente ya que al mismo tiempo forman parte de la aglomeración de depósitos. A medida que los aldehídos y las cetonas se incrementan en el lubricante por las reacciones de condensación, la viscosidad aparente del aceite comenzará a aumentar.
Los productos oxidados e insolubles (p) como el lodo y los depósitos son significativamente diferente a las moléculas que constituyen la mayor parte del lubricante. El lodo es la acumulación de insolubles, mientras que los depósitos son insolubles que se adhieren a la superficie metálica. Si los aditivos anticorrosivos se agotan, el agua y los ácidos promoverán la corrosión, lo cual es un subproducto de la oxidación.
En conclusión, los contaminantes como el agua, el oxígeno y las partículas metálicas tienen graves consecuencias sobre las máquinas y los lubricantes. Los antioxidantes pueden ayudan sustancialmente, pero eventualmente se agotarán durante el período de inducción.
Para que su lubricante dure más y sus máquinas operen por más tiempo, usted debe entender cómo se produce la oxidación.
olor sit amet, consectetur adipiscing elit. Ut elit tellus, luctus nec ullamcorper mattis, pulvinar dapibus leo.
Noria Corporation. Traducido por Roberto Trujillo Corona, Noria Latín América.














